第3号 特集:鉄の惑星・地球 Earth, the Iron Planet 铁之星球──地球
鉄に依存した赤血球による酸素輸送と人工赤血球
酒井宏水【奈良県立医科大学医学部化学教室・教授】
Iron-Dependent Oxygen Transport by Red Blood Cells and Artificial Red Blood CellsHiromi Sakai【Professor, Department of Chemistry, Nara Medical University】
依赖于铁的红细胞运氧和人工红细胞
──血の赤を決めているのは赤血球であり、さらにいえばそのなかに含まれるヘモグロビンだ。ヘモグロビン1分子に二価の鉄が4つ含まれ、それが酸素を運ぶ鍵になる。本論では、慢性的な輸血用赤血球製剤の不足や有事の際の血液の大量需要などを見据えた人工赤血球開発について、現時点での到達点を明らかにする。 (特集担当:伊藤孝)
[2021.10.4 UPDATE]
Hemoglobin is the most abundant metalloprotein in our blood. It consists of four protein subunits, and each has an embedded group called a heme, which contains a ferrous ion (Fe2+). In general, the color of aqueous solution with ferrous ions is light green or blue, but hemoglobin is reddish purple or red. The color differs due to the heme in hemoglobin. When ferrous ions are bonded with oxygen molecules (O2), it is red. When they are not, it is reddish purple. Red blood cells make up about 40 to 50 percent of our blood by volume, and that causes blood’s viscosity to be four times higher than water’s. The cells easily get oxygenated as the blood passes through capillaries of the alveoli, and after traveling from the heart to peripheral tissues through arteries, arterioles, and capillaries, they release oxygen. Then the cells return to the heart via venules and veins and are sent to the lungs to get oxygenated again.
The Japanese blood donation and transfusion system has the highest safety levels in the world, and it is indispensable for our current healthcare system. The supply for blood transfusion relies on donations from the public, therefore, changes in blood donation supply can potentially affect our healthcare system. Because the number of donations has declined due to the aging population and the COVID-19 catastrophe, the Japanese Red Cross Society and other medical institutions have been tirelessly making efforts to secure sufficient quantities of blood. Packed red blood cells for transfusion can be refrigerated for three weeks, which can limit the method of transportation and the amount of stockpiles. There are emergency situations where a patient suffering from critical bleeding cannot receive a transfusion.
As a solution to the problems in the blood transfusion system, we have developed artificial blood cells, Hb-vesicles (HbV), as artificial oxygen carriers, and studied their practical possibilities in diverse situations. We are able to purify hemoglobin solutions from unused red blood cells, provided by the Japanese Red Cross Society, that either expired or were unusable for other reasons. The solutions are encapsulated in microcapsules called liposomes, consisting of lipid molecules, to be processed into artificial red blood cells. The artificial red blood cells do not require cross-matching tests because they do not have blood types. In addition to this, the artificial red blood cells can be stored for a long period of time at room temperature, so they can be administered to anyone whenever there is need. The particle size of an artificial red blood cell is about 0.25µm. It is smaller than a real red blood cell, which is 8µm. For this reason, the artificial red blood cells are dispersed evenly in plasma and are able to carry oxygen through vessels that are harder for the real cells to penetrate. We have been studying the safety and efficacy of artificial red blood cells through experiments on various animals. In the experiments, we have confirmed that rats survive after replacing 90 percent of their circulating blood with artificial red blood cells. We also confirmed resuscitation in all of the experimental hemorrhagic shock models, in which 50 percent of circulating blood was rapidly removed from beagles and rabbits. Although the half-life of transfused artificial red blood cells is only a few days, they can function well enough as a bridge to a real blood transfusion operation in an emergency situation. Recently, we have begun clinical trials on safety.
Artificial red blood cells may not only be a substitute in transfusions. They have been found to be useful as an organ perfusion fluid and are effective for treatment of ischemic diseases and angioma laser treatment. Another thing is that hemoglobin binds to not only oxygen molecules (O2) but also carbon monoxide (CO). Generally, carbon monoxide is a toxic gas, but the toxicity is dose dependent. The studies on animals have shown that carbon monoxide can have positive effects in moderate doses, and carbon monoxide-conjugated artificial red blood cells work as antioxidant and anti-inflammatory agents.
There are many artificial organs being developed. Some of them have already been implemented. Since blood is called the “flowing organ,” blood transfusion can be considered a kind of organ transplant and artificial blood a kind of artificial organ. We are hoping that the artificial red blood cells can have widespread effects in future medical care by inspiring many new uses and treatments beyond the main use of transfusion.
1.鉄を含むヘモグロビンによる酸素輸送
血液中に存在する数多のタンパク質の中で最もたくさんあるのが、血色素「ヘモグロビン(hemoglobin)」である。ヘモグロビンは4つのサブユニットとよばれるタンパク質が集合しており、それぞれにヘム(heme)とよばれる二価の鉄イオン(Fe2+)をもつ物質が嵌まり込んでいる[fig.1]。一般にFe2+の水溶液は淡緑色や青色であるが、ヘムをもつヘモグロビンは赤紫色や赤色を呈する。酸素が結合していない状態では赤紫色で、4つのヘムのFe2+すべてに酸素分子(O2)が結合すると赤色になる[fig.2]。結合の様式は配位結合と呼ばれる。可逆的に結合(捕捉)と解離(放出)を繰り返すには、共有結合ではなく、結合力の弱い配位結合が必要である★1。
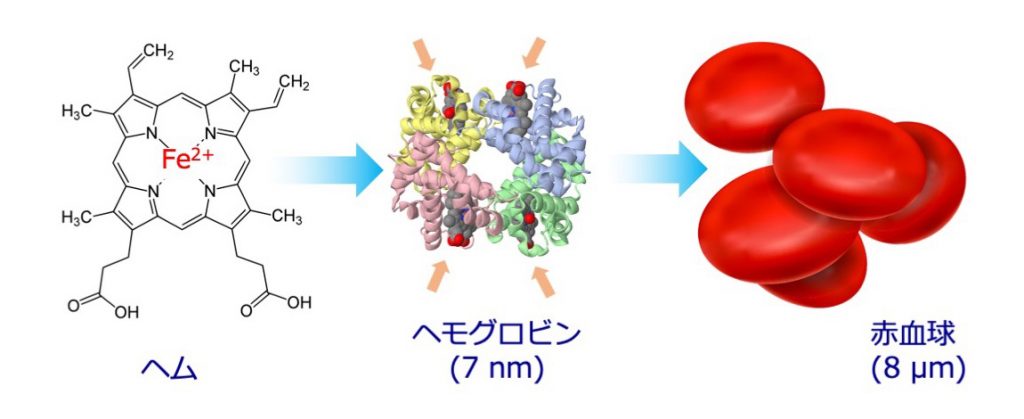
fig.1──鉄イオン(Fe2+)を含むヘムがヘモグロビンの4つのサブユニットそれぞれに嵌まり込んでいる。この鉄イオンに酸素が結合する。ヘモグロビンは赤血球内に約35wt%の濃度で封入されている。赤血球には核がなく、両凹円盤型の形状をしている。

fig.2──ヘモグロビンの色調の変化。酸素が結合したオキシヘモグロビンは赤色、酸素を除去したデオキシヘモグロビンは赤紫色をしている。毒ガスの一酸化炭素を結合したカルボニルヘモグロビンは鮮やかな赤色を呈し、英語でcherry redとよばれる。筆者撮影
このヘモグロビンは、赤血球の中に濃度高く封入されている(約35g/dL)。赤血球は細胞のひとつであるが、哺乳類の赤血球には細胞核が欠如している。進化の過程で細胞核を捨て、酸素輸送に特化した細胞といわれている★2。赤血球は球形ではなく、両凹円盤型の構造をとり、長径は約8ミクロン、厚さは2〜3ミクロン程度である。毛細血管の内径は4〜5ミクロン程度と細いが、球形でない赤血球はその形態を自在に変化させ、自身の径よりも細い毛細血管の中を速やかに通過することができる。赤血球の総体積は血液の約40〜50%をも占めるため、血液の粘度は水の4倍もあるが、血液が肺胞の毛細血管を通過するときに容易に酸素化され、心臓から送り出され動脈を経由して末梢組織に運ばれて酸素を放出する。そして静脈を経て心臓に戻り、肺に送られ再酸素化される。ヘモグロビンの血中濃度(12〜15g/dL)は、血液中のあらゆるタンパク質の濃度よりも高く、体内への酸素供給が生命の維持に如何に重要であるかを示している。
2.多くの生物は鉄を選んだ
鉄イオンを含む「ヘムタンパク質」に分類されるヘモグロビンは、ほぼすべての脊椎動物と一部の無脊椎動物や昆虫などの血液に含まれる★3。細菌や植物中にも検出される場合がある。同じくヘムタンパク質に分類されるミオグロビン(myoglobin)も酸素分子を結合し、骨格筋や心筋などの成分であり、赤色を呈する要因である。血液や筋肉の赤色は生命力を表す色であり、ヒトは本能的に赤色に反応し、情熱、活力、ときに興奮、怒りを感じさせ、青色の印象と対照的とされる。「鉄血」や「鉄筋」という言葉があるのも結びつきの強さを物語っている。このほかにもヘムタンパク質には幾つもの種類があり、生体内の酸化還元反応を担う酵素などとして、多くの生物の臓器に含まれている。ヒト体内には約2〜4gの鉄が存在しているという。生命維持に重要な酸素運搬や化学反応を継続するために、多くの生物は進化の過程で鉄(Fe)を利用することを選択してきた。例えば貧血気味のときに赤々としたマグロの刺身、牛肉や鯨肉を食べるよう勧められたり、南部鉄鍋を使って料理したらいいと勧められたり、これらはすべてヘモグロビンの構成要素となる鉄分の補充が目的である。スポーツ選手が禁止薬物エリスロポエチンを使うドーピングは、赤血球を増やして酸素運搬効率を高めることを期待したものである。鉄と同じ遷移元素に、レアメタル(希少金属)のひとつ、コバルト(Co)がある。ヘモグロビンの鉄イオン(Fe2+)を人為的にコバルトイオン(Co2+)に置換した研究の報告によれば、酸素分子を配位結合するものの、その結合力は鉄イオンの場合の10分の1程度に低下する★4。また色調も微妙にFe2+の場合とは異なる。他方、軟体動物と節足動物(タコ、イカ、エビ、クモ、カブトガニなど)の類は、進化の過程で遷移元素の中から銅(Cu)を選択し、銅イオンを含むヘモシアニン(hemocyanin)という青色のタンパク質を酸素運搬のために利用している★5。この場合も酸素分子が銅イオン(Cu2+)に配位結合する。現在、地球上で栄華を極める脊椎動物が生命維持に必要な大量の酸素を体内に取り込むために、地球上に圧倒的に多く存在する鉄(Fe)を選択してきたことは、理に叶っている。もし、地球上に圧倒的に銅が多く存在していたら、生物の多くは銅を含むヘモシアニンを選択し、ヒトの血液は青く、赤色と青色に対する印象も違っていたかもしれない★6。
脊椎動物の中に例外がある。ヘモグロビンを持たない魚である。コオリウオという南極の凍るほど冷たい海域に生息する魚である★7。コオリウオの血液は無色で、その体積は通常の魚の4倍もあるという。酸素の水に対する溶解量は、低温になるほど大きくなる。大気下37℃の水の酸素溶解量は約7mg/Lであるが、1℃の水は2倍の約14mg/Lになる。コオリウオは大きな心臓を使って酸素が溶けた無色の血液を全身に送り、また鰓(えら)だけでなく体表面からも酸素を取り入れることができる。コオリウオは進化の過程で酸素溶解量の高い冷たい海水の中で生きることを選択し、不要なヘモグロビンを捨ててきた。そのため海水温が上がれば酸素欠乏により死んでしまう。対してヒトの血液には、37℃で約300mg/Lの酸素が含まれている。上述の7mg/Lのじつに40倍もの酸素を含有している。これはヘモグロビンが血液中に濃度高く存在することで達成されている。体積に換算するとヒト血液1Lあたり約245mLの気体の酸素を溶解していることになる。血液は一回の循環でその約25%の酸素を末梢組織に放出する。1分あたりの心拍出量は4〜5L程度で、成人の1分あたりの酸素消費量約230mLを供給している。ヒトは生命の維持に実に多くの酸素を必要としている。
3.赤血球輸血とその課題
体重の約13分の1が血液の重量なので、体重が65kgのヒトは丁度5000mLの血液を持つ計算になる。献血をした経験があればご存知の通り、以前は200mL採血であったが、現在では400mL採血が主流になってきた。つまり出血量が400mL程度のときは生死にはまったく影響はない。生体にはこの程度の出血に対処するだけの余力を備えている。しかし、出血量が1000mLを超えると、電解質溶液などの輸液が必要になり、またさらに出血が進んだ場合には直ちに赤血球を輸血して酸素供給を補う必要が出てくる。大量出血になると、細胞レベルで酸素が不足する事態に陥る。外傷、母体出血、胃腸出血、手術中の出血、動脈瘤の破裂など、出血の原因は幅広い。大量出血が起きた場合、30分後の死亡率は50%、1時間で100%が死亡するという。この1時間をゴールデン・アワーという。致命的な外傷を負った場合では、より短時間で死亡率100%に達する。出血による死亡は世界的な問題で、全世界で年間1,900万人が死亡しており、そのうち150万人は外傷が原因と報告されている★8。
輸血用血液の供給は、国民の善意による献血に依存している。わが国の献血─輸血システムの安全性は世界最高水準にあり、現行医療に不可欠である。しかし、幾つかの課題を抱えている。輸血を介したウィルス感染(肝炎、エイズなど)は、採血液のウィルス検査と献血者に対する問診の充実により現在ではほとんどなくなっているが、既知の病原性ウィルスすべてについて検査することはコスト的に出来ないであろうし、新興ウィルスの脅威にも晒されている。また、新型コロナウィルス感染症の蔓延に対し、政府が緊急事態宣言を発令した後、外出を控えるようになったため献血者数が急減したことが報道された★9。献血─輸血システムに依存している医療は、輸血用血液の供給体制に何か変化があると、大きな影響を受ける可能性がある。そして少子高齢化により献血者数が低下している状況にもあり、日本赤十字社をはじめ医療機関の現場では、十分量の血液を確保するため不断の努力が続けられている。広く献血の協力が呼びかけられ、国民の関心も高い★10。
しかし、輸血用赤血球製剤の保存期間は冷蔵で3週間であり、輸送手段や備蓄量に限界が生じることがありうる。危機的出血にある傷病者に対し輸血をしたくても輸血が極めて困難となる状況がある。離島・へき地医療、夜間救急、緊急手術の現場では、輸血用血液を確保できないときがあると聞く。患者の血液型と合致する輸血用血液が不足することもある。プレホスピタル(病院前救護)の現場では、救急救命士が重度傷病者に対して輸血することはできない。周産期管理の進歩により母体死亡率は著明に低下したものの、出血は依然、母体死亡の主要な原因とされている★11。通常の分娩でも大量出血は起こりうるため、予期せぬ大量出血の対応が遅れ、搬送中に心停止する事例が報告されている。大規模自然災害(東南海トラフ、首都直下型地震)、テロ、あるいは有事の際、輸血用血液の大量需要と迅速な供給にどう備えるか、危機管理対応策が必要とされている。
4.人工赤血球とは
このような献血─輸血システムの抱える課題の解決策のひとつになればと考え、著者らは人工赤血球(ヘモグロビンベシクル、HbV)を開発し、酸素運搬体として使用できるかどうか、可能性を多角的に追求してきた[fig.3]★12。日本赤十字社から譲り受けた非使用赤血球(期限切れ、検査落ち)をもとに、ヘモグロビン溶液を精製することができる。これをリポソームとよばれる脂質分子が構成する微小カプセルに封入し、人工赤血球に加工する。ナマモノである赤血球の保存期間は、日本では採血後冷蔵で3週間、欧米では6週間とされている。保存時間が長くなると、酸化劣化が進みとくに生体膜が破壊され、ヘモグロビンが赤血球から漏出する溶血が起こる。タンパク質は一般に熱に弱い物質であるが、ヘモグロビンは条件を選べば極めて安定で、60℃加熱処理によるウィルス不活化などを経て簡単に精製単離することができ、人工赤血球の原料として使用できる。献血液は日本赤十字社が特定のウィルス検査(NAT検査)をしてウィルスがないことを確認しているが、ヘモグロビンの精製工程を経て感染に対する安全性をさらに高めることができる。

fig.3──人工赤血球の色調比較。何も結合していない状態のdeoxy-HbVと、一酸化炭素が結合したCO-HbV。Deoxy-HbVは血管内投与されると肺で酸素化され、末梢組織に酸素を供給する。CO-HbVは血管内投与されるとCOを放出した後、酸素運搬体に変換される。放出されたCOは細胞保護効果を呈する。どちらも室温で長期間保存ができる。筆者撮影
また、ABO式血液型抗原は赤血球膜に存在するので、赤血球膜を除去した精製ヘモグロビンには最早、血液型物質は存在しない。しかしヘモグロビンは本来、赤血球の中に入った状態で存在しており、溶血により外に放出されるとさまざまな毒性を呈する。そこで、このヘモグロビンを濃縮してリポソームに封入し人工赤血球とする必要がある。人工赤血球製剤には血液型はなく、交叉試験を必要としない。また、人工赤血球製剤は、室温で長期間備蓄することができ、必要時にいつでも誰にでも投与できる。人工赤血球の粒子径は約0.25µmで、赤血球(8µm)よりも小さく血漿中に均一に分散し、赤血球が透過しにくい血管も通過して酸素を輸送できる[fig.4]。この人工赤血球製剤について、これまでにさまざまな動物実験により安全性と有効性の確認を進めてきた。実験的には、循環血液量の90%を人工赤血球で置換してもラットが生存すること、ビーグル犬やウサギを用いた循環血液量の50%を急速に脱血する出血性ショックモデルに対する投与でも、全例が蘇生されることを確認している★12。人工赤血球製剤の半減期は数日程度であるが、緊急時に投与して輸血治療までの繋ぎとして十分に機能するものと考えている。最近、ようやく臨床試験(安全性試験)を開始したところである。
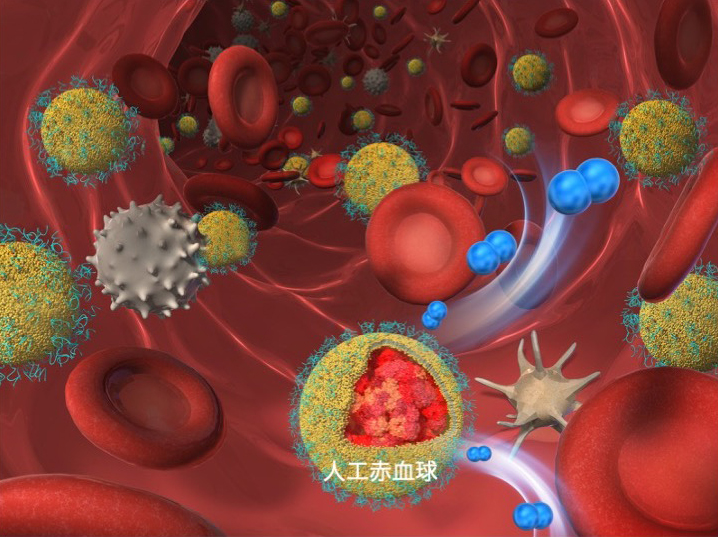
fig.4──血管内を流動する血球成分と人工赤血球のイメージ図
歴史的には、ヘモグロビンを利用した人工赤血球、人工酸素運搬体の研究開発は1950年代から始まり、ヘモグロビンをカプセル化したものだけでなく、ヘモグロビンどうしを結合させたり、水溶性高分子を結合させて大きくしたものなど、世界中で多くの研究者が取り組んでいる★13。ヒト由来のヘモグロビンだけでなく、ウシ、ブタなど家畜由来のヘモグロビン、ゴカイやミミズがもつ巨大ヘモグロビン、遺伝子組み換え技術により大腸菌が産生したヒト型ヘモグロビンなどの利用も検討されている。このほか、パーフルオロカーボン(PFC)を使った酸素運搬体も知られている。これは、PFCの液体が水に比較して非常に高い酸素の溶解性を示すことを利用している。PFCは、テフロンのような炭素とフッ素の化合物のひとつで、低分子量のため常温で液体である。水と馴染まないので、脂質を加えて生理食塩水中で乳濁させて微粒子として血管内に投与することができる。日本でも実用化されたことがあったが、酸素運搬量が十分でなく、また肺に対する副作用が問題で、製造中止となった。現段階では、人工赤血球、人工酸素運搬体の開発の主流はヘモグロビンを利用する形式といえる★14。
人工赤血球は、輸血代替としての利用のみならず、臓器灌流液としての利用や、虚血性疾患の治療、血管腫レーザー治療にも有効であることが解ってきた★15。また、ヘモグロビンは酸素分子(O2)だけでなく一酸化炭素(CO)も結合する。一酸化炭素は毒ガスであるが、その毒性は量の問題であり、どのような物質も(例えば水でも塩でも)多量に摂取すれば毒性を示す(鉄も鉄過剰となれば毒性を示す)★16。一酸化炭素は適量であれば効能を示し、一酸化炭素を結合した人工赤血球に、抗酸化的、抗炎症的な作用があることが動物投与試験から明らかになっている。
5.おわりに
生命の進化の過程で、脊椎動物は銅でもなく、コバルトでもなく、地球上に圧倒的に多く存在する鉄を選択してきた。鉄を含有するヘモグロビンなくして可逆的な酸素の結合と解離は為し得ない。そしてヘモグロビンが赤血球の中に封入され体内の酸素輸送の役割を担い、生命の維持に不可欠の要素となっている。献血─輸血システムは現行の医療を支える重要な技術である。使われずに廃棄される赤血球から精製したヘモグロビンを利用した人工赤血球製剤は、輸血治療を補完する製剤として期待されている。体内の多くの臓器に対して「人工臓器」が開発され、実用化されているものもある★17。血液は「流れる臓器」ともよばれ、輸血は臓器移植のひとつ、人工血液は人工臓器のひとつともいえる。人工赤血球は輸血代替のみならずさまざまな新しい利用法が提案され、将来、医療を大きく変革させるきっかけになるのではと期待しているところである。
参考文献
★1──“Hemoglobin: Molecular, Genetic and Clinical Aspects” Eds. by H.F. Bunn & B.G. Forget, W.B. Saunders Co., Philadelphia, PA, 1986
★2──ビクター・W・ロッドウェル『イラストレイテッド ハーパー・生化学 原書30版』「第6章:タンパク質:ミオグロビンとヘモグロビン」「第53章:赤血球」(清水孝雄監訳、五十嵐和彦ほか訳、丸善出版、2016)(https://www.maruzen-publishing.co.jp/item/?book_no=295065)
★3──梶田昭彦+五十嵐吉彦+吉田裕明「無脊椎動物の血色素」(『蛋白質核酸酵素』32(6), 496〜518頁、共立出版、1987)
★4──Yonetani T, Yamamoto H, Woodrow III GV. “Studies on cobalt myoglobins and hemoglobins”, J Biol Chem, 249(3), 682-690 (1974)
★5──加藤早苗+松井崇+田中良和「23.8 MDaの超巨大酸素運搬タンパク質ヘモシアニン会合体の結晶構造」(『生化学』90(2)、238〜243頁、日本生化学会、2018)https://seikagaku.jbsoc.or.jp/10.14952/SEIKAGAKU.2018.900238/data/index.html
★6──Nature picture library. Horseshoe Crab (Limulus polyphemus) blood which is blue due to copper-based hemocyanin and is widely used in the medical field, Delaware. https://www.naturepl.com/stock-photo-limulus-polyphemus-nature-image00476987.html
★7──多田諭「透明な血液をもつ南極の魚「コオリウオ」公開!」(葛西臨海水族館 東京ズーネット、2011年8月24日)(https://www.tokyo-zoo.net/topic/topics_detail?inst=kasai&link_num=19672)
★8──Cannon JW,“Hemorrhagic Shock”, New Engl J Med, 2018;378:370-9. https://www.nejm.org/doi/full/10.1056/NEJMra1705649
★9──Stanworth SJ, et al., Effects of the COVID-19 pandemic on supply and use of blood for transfusion. Lancet Haematol. 7(10), e-756-e764, 2020. https://doi.org/10.1016/S2352-3026(20)30186-1
★10──松坂俊光「我が国の献血の現状と課題」(『日本輸血細胞治療学会誌』59(5)、725〜732頁、日本輸血・細胞治療学会、2013)(https://doi.org/10.3925/jjtc.59.725)
★11──産科危機的出血への対応ガイドライン(https://www.jspnm.com/topics/data/topics100414.pdf)
★12──拙論「人工赤血球(ヘモグロビン ベシクル)製剤の新しい利用法」(『日本輸血細胞治療学会誌』64(4)、589〜596頁、日本輸血・細胞治療学会、2018)(https://doi.org/10.3925/jjtc.64.589)
★13──“Nanobiotherapeutic Based Blood Substitutes”. Eds. by T.M.S. Chang, L. Bülow J. Jahr, H. Sakai, C. Yang, World Scientific Publishing Co. Pte. Ltd., Singapore, 2021. https://www.worldscientific.com/worldscibooks/10.1142/12054
★14──The 17th International Symposium on Blood Substitutes and Oxygen Therapeutics (Nara, Japan, Nov.21-23. 2019). https://www.blood-sub.jp/file/XVII-ISBS-2019.pdf
★15──H. Sakai. “Overview of potential clinical applications of hemoglobin vesicles (HbV) as artificial red cells”, evidenced by preclinical studies of the academic research consortium. J. Funct. Biomater. 8, 10, 2017 https://doi.org/10.3390/jfb8010010
★16──高後裕+大竹孝明「鉄代謝の生体に及ぼす影響」(『外科と代謝・栄養』49(2)、59〜65 頁、日本外科代謝栄養学会、2015(https://doi.org/10.11638/jssmn.49.2_59)
★17──日本人工臓器学会ホームページ「人工臓器とは?」(https://www.jsao.org/public/what/)
1966年生まれ。医用生体工学・生体材料学。奈良県立医科大学医学部化学教室 教授、博士(工学)・博士(医学)。1994年 早稲田大学大学院理工学研究科修了(高分子化学)、1996年 カリフォルニア大学サンディエゴ校 生体工学部留学、2006年 慶應義塾大学大学院医学研究科 博士(医学)。現在 AMED「備蓄・緊急投与が可能な人工赤血球製剤の実用化を目指す研究」代表者。日本血液代替物学会 会長。主な著書=『Nanobiotherapeutic Based Blood Substitutes 』(共編著、World Scientific Publishing Co. Pte. Ltd.、2021)など。
- 3号の読み方:鉄はいつでもそこにある
-
How to read No. 3: Iron is always there
/阅读指南:从未缺席的铁
伊藤孝/Takashi Ito - インタビュー:アナトリア──文明と鉄の関係の幕開け
-
Anatolia and the Origins of the Relationship between Iron and Civilization: An Interview with Sachihiro Omura
/访谈:安纳托利亚——文明与铁关系的拂晓
大村幸弘/Sachihiro Omura - 鉄と生命──鉄はなぜ生命に選ばれたのか
-
Role of Iron in Life: A Review
/铁与生命——铁为什么选择了生命
高萩航+北台紀夫/Wataru Takahagi+Norio Kitadai - 鋼の構築様式
-
Steel and the Origin of Building Mode 3
/钢铁的构筑方式
中谷礼仁(文)+松田法子(図)/Norihito Nakatani+Noriko Matsuda - 鉄に依存した赤血球による酸素輸送と人工赤血球
-
Iron-Dependent Oxygen Transport by Red Blood Cells and Artificial Red Blood Cells
/依赖于铁的红细胞运氧和人工红细胞
酒井宏水/Hiromi Sakai - インタビュー:鉄・生命・メタ生物圏
-
Interview: Iron, Life, and the Metabiosphere
/采访:铁・生命・元生物圈
長沼毅/Takeshi Naganuma
協賛/SUPPORT サントリー文化財団(2020年度)、一般財団法人窓研究所 WINDOW RESEARCH INSTITUTE(2019〜2021年度)、公益財団法人ユニオン造形財団(2022年度〜2024年度)、石灰石鉱業協会(第9号)




